·“在结构生物学领域,解析生物大分子的柔性结构是一个长期目标。复旦团队开发的新算法使科研人员能通过冷冻电子显微镜看到关键的结构细节,这是以往技术无法实现的,将对生物学、化学研究和药物发现产生重要影响。”
计算生物学再次迎来突破,生物大分子结构解析精度得到升级。
近日,复旦大学复杂体系多尺度研究院院长马剑鹏教授领衔的科研团队开发出了新型智能计算方法OPUS-DSD,该算法不但能够成功地解析在冷冻电子显微镜(Cryo-EM)结构解析技术中,因传统方法无法分辨而缺损的生物大分子(比如蛋白质、核酸或蛋白质/核酸复合物等)结构,还能高效精准地分辨出生物大分子的柔性结构域在受测样品中的构象分布。
据悉,这一新方法能有效建立高精度的生物大分子结构模型,帮助解决药物设计中因目标蛋白结构不准而导致的新药研发失败问题。
北京时间10月9日晚,相关论文“OPUS-DSD: deep structural disentanglement for cryoEM single-particle analysis”刊发在《自然-方法》(Nature Methods,影响因子47.99)杂志。

论文已发布在《自然-方法》(Nature Methods)杂志。图片来源:《Nature Methods》
2013年诺贝尔化学奖得主、复旦大学复杂体系多尺度研究院荣誉院长迈克尔·莱维特(Michael Levitt)表示:“在结构生物学领域,解析生物大分子的柔性结构是一个长期目标。复旦团队开发的新算法使科研人员能通过冷冻电子显微镜看到关键的结构细节,这是以往技术无法实现的,将对生物学、化学研究和药物发现产生重要影响。”
生物大分子结构解析是基础生物科学的关键技术之一,冷冻电镜是其中非常重要的一种研究手段。目前,中国具有世界上最大的冷冻电镜设备集群,然而大部分数据处理所需的软件仍依赖进口。要确立高精度结构模型,就必须发展自主、先进的冷冻电镜数据处理智能算法。
据研究人员罗镇威介绍,生物大分子的许多重要功能是通过其高度的柔性特质来完成的,但柔性也是干扰结构测定精度的主要因素。在处理冷冻电镜数据的过程中,生物大分子结构柔性引起的构象多样性使得从单个样本中获取精确的三维模型充满挑战。同时,由于冷冻电镜实验数据的信噪比通常极低,为深度学习算法在该领域的运用带来了巨大困难。如何克服冷冻电镜数据中生物大分子结构的柔性、尤其是超大型复合物的柔性对结构测定精度带来的误差,是当前全球结构生物学研究的重点和难点,也是亟待打破的“瓶颈”。
复旦大学最新开发的智能算法OPUS-DSD,成功地攻克了以上难题。研究团队推出了一种基于深度学习的计算方法,可有效地识别和处理生物大分子的柔性信息,从而提高冷冻电镜的解析能力,并获取生物大分子三维结构的动态变化信息。
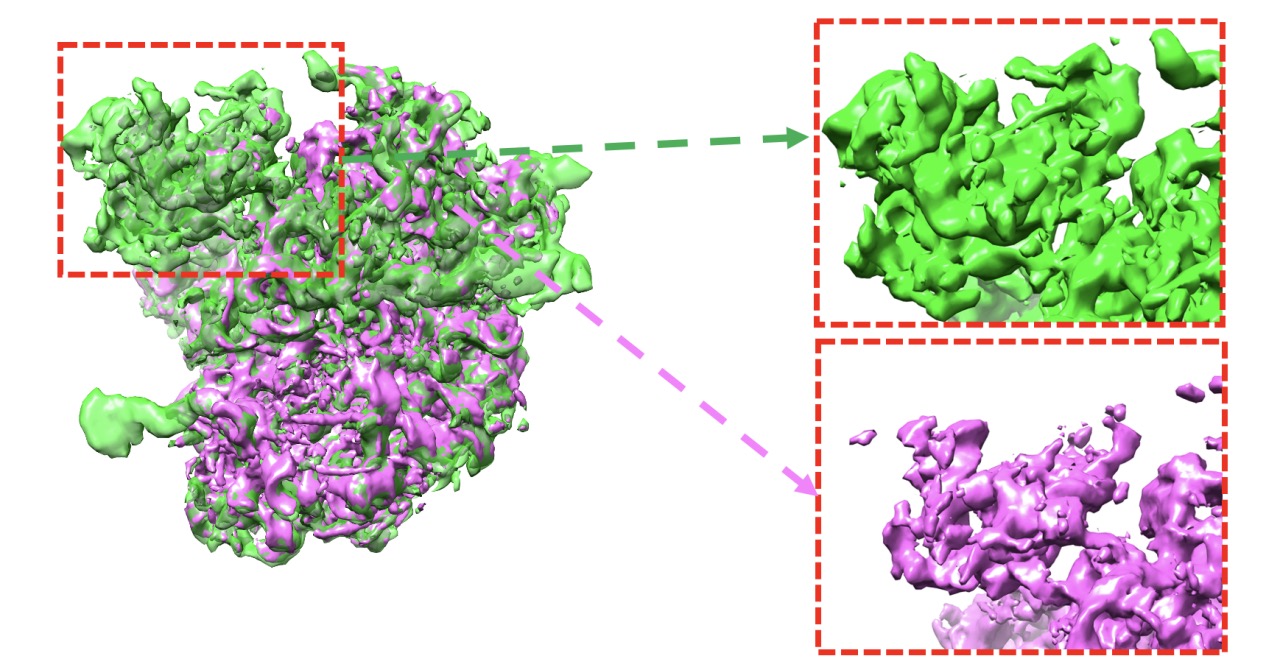
OPUS-DSD重构结构模型与传统冷冻电镜软件解析的模型对比。在虚线标示的区域中,OPUS-DSD重构的模型(绿色)比传统冷冻电镜软件解析的模型(紫红色)有更加完整的电子密度。图片来源:《Nature Methods》
据介绍,OPUS-DSD具有卓越的数据处理能力和鲁棒性(指某个系统或者算法对于随机噪声、异常情况和攻击等意外干扰的抗干扰能力),能在更低信噪比的数据上保持较高的解析准确性。此外,它不仅仅局限于单颗粒冷冻电镜技术,也可推广到更高端更低信噪比的冷冻断层扫描电镜(Cryo-ET)的研究中。
论文通讯作者马剑鹏教授指出:“优秀算法的研究,绝非一日可就,难度极大,耗时漫长,需要研究人员有坐长期冷板凳的勇气,每一个大的进步,往往都需要很多很多年的积累。”
研究人员表示,未来,团队将继续以人工智能为技术中枢,构建新一代生物体系分析工具与方法,解读生物遗传信息,加速生命科学在分子层面的研究。通过对蛋白质、核酸等生物大分子功能结构的预测与设计,为药物研发提供支持,支撑全链条AI-赋能新药研发的先进技术平台。
论文链接:https://www.nature.com/articles/s41592-023-02031-6 ,算法在GitHub开源:https://github.com/alncat/opusDSD。

新闻热点
新闻爆料